Samspillet mellom cardiac output og SVR fører til et blodtrykk. Blodtrykket distribuerer så CO videre til organene. Så lenge blodtrykket er adekvat, vil hvert organ autoregulere sin perfusjon gjennom lokal vasodilatasjon. Hensikten med cardiac output er å skape nok trykk og nok flow slik at alle organer kan styre sin egen perfusjon. Ingenting annet.
Anemiske pasienter får ofte veldig god blodtrykksrespons av SAG. Dette er ikke fordi SAG er et kolloid; for at noe skal være et kolloid må de være oppløst i væske og dermed osmotisk aktiv. Røde blodceller er ikke oppløst i blod. Derimot har de høy viskositet og øker resistens og øker dermed BT hvis folk er anemiske. Denne SVR-effekten vil føre til blodtrykksøkning uavhengig av slagvolum eller volumstatus og vil finne sted også hos de som ikke er volumrespondere.
Ved blødning tar det 8-12 timer før Hb faller. Dette var lengre enn jeg trodde. En «umiddelbar» transkapillær refylning skjer fremdeles, men dette har lite effekt på Hb.
All tilnærming av væskebehov, NorA-behov, oliguri og volumstatus tar utgangspunkt i om vevsperfusjon er redusert eller ei. Dette er vurdert klinisk, men ScvO2, Pv-aCO2, laktat og kapillærfylning er markører på at det er reduesrt. CNS funksjon og oliguri kan også brukes, men har flere konfoundere.
Pmsf (mean systemic filling pressure) representerer kroppens stresset volum som sørger for drivtrykket til venøs retur. Dette trykket har vært vanskelig å måle fordi det forutsetter sirkulasjonsstans. Mend et er en måte å måle Pmsf på ved hjelp av arteriekran og en blodtrykksmansjett: Man blåser opp blodtrykksmansjetten på samme arm som arteriekran. Oppblåsingen må skje raskt, for å unngå arteriell innstrøm mens venøs utstrøm blokkeres. Hvis dette gjøres riktig, kan man lese av trykket på arteriekranen, som vil tilsvare Pmsf og dermed det stressede volumet.
Selv om pasienten er volumresponder og hypotensiv, er det ikke sikkert at blodtrykket vil øke når vi gir væske. Det er fordi vasodilatasjon skaper høy compliance i arterietreet. Compliance = delta_volum/delta_trykk. Dermed vil ikke økning i slagvolum føre til økning i blodtrykk. Hvis man måler slagvolumvariasjon (SVV) óg pulstrykkvariasojn (PPV) kalles forholdet mellom disse to (PPV/SVV) for dynamisk arteriell elastance (Eadyn). Eadyn < 0.9 taler for at blodtrykket ikke vil øke, tross økt slagvolum. Eadyn > 0.9 taler for at noradrenalin kan trappes ned uten at blodtrykket faller.
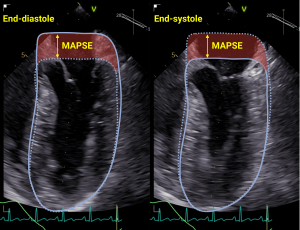
Hele denne generasjonen med anestesileger kommer til å være ekkokompetente.
Volumtoleranse er et annerkjent begrep.
Hjertets energitilføresel er en forutsetning for hjertets oksygenforbruk (MVO2). MVO2 omsettes til cardiac power output (CPO), som bare er produktet av MAP og CO. CPO linkes så til DO2 for å matche kroppens VO2. Ved kardiogent sjokk er det både mismatch mellom hjertets energitilførsel og MVO2 (=iskemi, ofte supply-demand), i tillegg til en mismatch mellom omsatt CPO (hypotensjon, lav CO) og kroppens VO2 (sjokk). Knutepunkter mellom kroppen og hjertet blir dermed CPO og MVO2. Forholdet mellom CPO/MVO2 er cardiac efficiency; forholdet mellom energi investert og utbytte, eller hvor mye valuta kroppen får for pengene hjertet bruker. Efficiency kan undersøkes gjennom ventrikulo-arteriell kobling (VA-coupling).
Ea er forkortelsen for arteriell elastans, og er en god markør for afterload. Det har en lang matematisk formel, men koker ned til SVR ganger puls. I senere tid ble det oppdaget en enklere måte å beregne Ea med formelen Ea = 0.9*systolisk BT/slagvolum, og kan måles i klinisk praksis. Ea representerer afterloadkomponenten i VA-coupling, der Ees er venstre ventrikkels kontraktilitet. Ees er dessverre ikke enkel å måle i klinisk praksis. VA-coupling er brøken Ea/Ees, og er vanligvis mellom 0.6 – 1.
VA-ECMO gir retrograd flow i aorta og øker afterload til venstre ventrikkel, og dermed hjertets oksygenforbruk (MVO2). Likevekten mellom flow ut fra venstre ventrikkel og retrograd flow fra ECMO skaper et vannskille. Dersom høyre ventrikkel pumper gjennom lungekretsløpet, vil respirasjonssvikt føre til at deoksygenert blod havner proksimalt for vannskillet. Koronarene er mest utsatt, fordi de sitter mest proksimalt. Dette kan overvåkes med pulsoksiometer på høyre arm.
MINS og perioperativ hjerteinfarkt er et anerkjent problem, men sykehuset har foreløpig ingen systemer for dette. Anestesilegen forlater pasientansvaret etter PO/recovery, kirurger er mest opptatte av det kirurgiske, og kardiologer har ikke kapasitet til å håndtere denne arbeidsmengden. Denne pasientgruppen blir dermed neglisert og postoperativ dødelighet forblir høy.
Gassanestesi er bedre for hjertet enn TIVA, ikke fordi det er mer hemodynamisk stabilt, men fordi det har en beskyttende effekt og fører til mindre troponinutslipp.
Fentanyldoser for hjerteinnledning: 10-20 mcg/kg.
Pulmonalarterietrykket (PAP) fra Swan-Ganz kateteret må tolkes i lys av cardiac output. I kontekst av lav CO kan et mild-moderat økt PAP forklare at årsaken til lav CO skyldes økt RV afterload. Hvis man har ligningen for PVR i bakhodet vil man oppdage dette: PVR = 80*mPAP-PAOP/CO. Lav CI og mild-moderat PAP vil gi høy PVR og dermed avsløre høy RV afterload og høyresvikt.
Tips til mer stabil TCI-narkose for eldre ASA 3+ pasienter: bruk muskelrelaks. De sovner på lave doser TCI, men er ofte litt for stive for god luftveishåndtering og kirurgi. Litt relaks løser dette, uten at de blir overdosert med anestesi og uten awareness.
Intuber dritsyke pasienter med sirkulasjonssvikt óg respirasjonssvikt. Dyspné og tachypnea forverrer DO2/VO2-balansen betydelig, spesielt ved sjokk der DO2 allerede er utilstrekkelig. Narkose, muskelrelaks og intubasjon reduserer VO2 og dermed kan sirkulasjonssystemet få mindre arbeidsoppgaver.
Høyresvikt fortjener respekt, men ikke frykt. Ikke la høyresvikt lamslå deg fra å intubere pasienten med ARDS.
Septisk sjokk kan ha høyresvikt, også uavhengig av ARDS og ventilatorinnstillinger.
De fleste komplikasjonene fra Swan-Ganz kateter er brukerfeil: pulmonalarterieruptur fordi ballongen blåses opp for perifert, lungeinfarkt fordi kateteret obstruerer flow, kateterknute fordi man mater og mater inni høyre ventrikkel. Resten er som komplikasjoner ved CVK: infeksjon, arteriepunksjon og pneumothoraks.
Verdien i PiCCO er transpulmonal termodilusjon. Dermed er PiCCO en diagnostisk undersøkelse og ikke kontinuerlig monitorering. Repeterte undersøkelser er nyttig, men krever jobbing og tilstedeværelse.