Pulstrykkvariasjon (PPV) forteller om noe volumstatus hos intuberte pasienter og er tilgjengelig for alle pasienter med arteriekran. PPV > 12 taler for at pasienten er væskeresponder; dvs. pasientens cardiac output vil øke med > 10% dersom du gir et væskebolus på 500mL. PPV < 12 taler for at pasienten ikke er væskeresponder (1). Dersom pasienten ikke er væskeresponder, er han i alle fall ikke hypovolem. Hvis pasienten er væskeresponder, er ikke dette et tegn på hypovolemi – å respondere på væske er normal fysiologi. Mange forkaster PPV fordi de mener den har for mange begrensninger, men i det siste har det kommet nye varianter av PPV som kan overkomme disse begrensingene. Dette betyr at vi kan overvåke preload uten ekko eller annen avansert hemodynamisk monitorering.
Hvordan få PPV på Philips monitor
- Aktiver PPV og bekreft.
- Endre PPV-kilde fra ABP til ART. Da vil PPV bli «På».
- Få en plass på skjermen: Trykk et sted og «Endre tallverdi» og finn PPV.
Fysiologien bak PPV
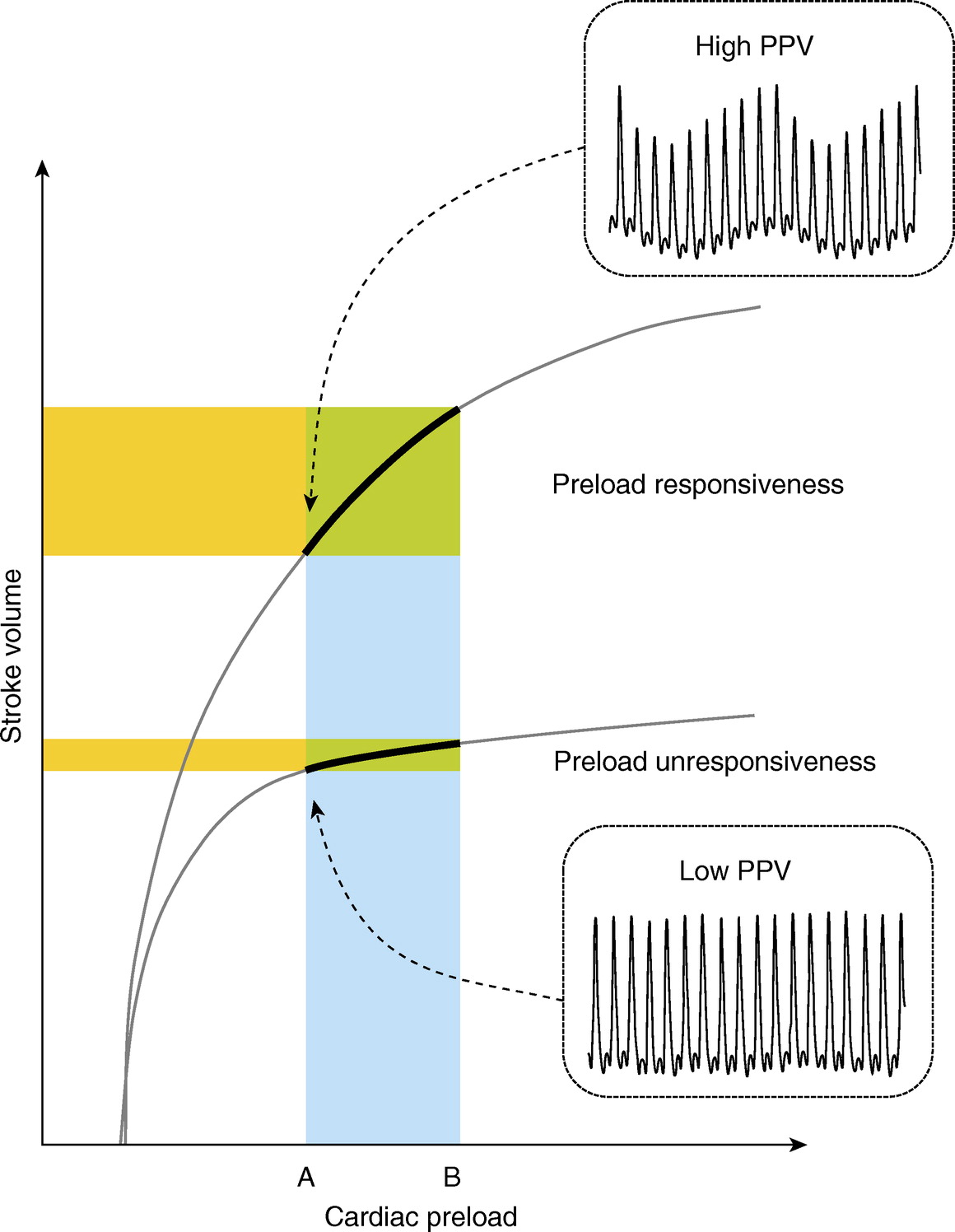
Slag-til-slag variasjoner i pulstrykket forteller om slag-til-slag variasjoner i slagvolum. Dermed kan vi sette pulstrykket på Y-aksen i Frank-Starlingkurven. På X-aksen finner vi, som vanlig, preload. Hver gang ventilatoren gir et tidalvolum så faller preload. Hvis pasienten er på den bratte delen av Frank-Starlingkurven, vil fall i preload føre til fall i pulstrykk – og dermed pulstrykkvariasjon når ventilatoren så slipper opp (2). Jo lengre til venstre man er på kurven, jo høyere PPV får man. Det motsatte er også sant: jo lengre til høyre, jo lavere PPV.
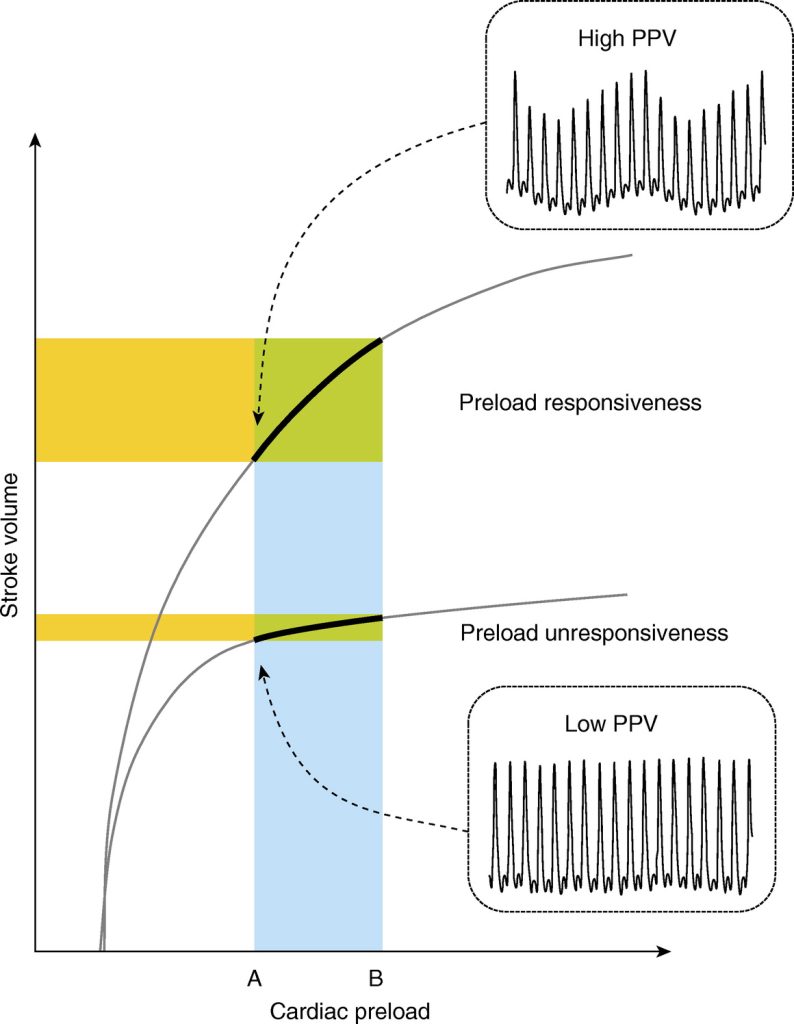
https://www.atsjournals.org/doi/abs/10.1164/rccm.201801-0088CI
Published in: Jean-Louis Teboul; Xavier Monnet; Denis Chemla; Frédéric Michard; Am J Respir Crit Care Med 19922-31.
DOI: 10.1164/rccm.201801-0088CI
Copyright © 2019 by the American Thoracic Society
PPV og tidal volume challenge
Så lenge vi setter tidalvolum (Vt) til 8mL/kg vil de fleste pasientene på til operasjonsanestesi oppfylle de fysiologiske vilkårene for å bruke PPV. Dersom tidalvolum (Vt) < 8mL/kg kan det bli for lite endring i preload mellom hver respirasjonssyklus, og dermed blir PPV lavere og kan i slike tilfelles ikke utelukke at pasienten er væskeresponder. Fordi Vt < 8mL/kg er obligatorisk for alle intensivpasienter er det mange som forkaster PPV. Men i de siste 5 årene har det kommet en løsning på dette: tidal volum challenge.
Tidal volume challenge gjennomføres i praksis ved at vi setter Vt på 6 mL/kg, noterer oss PPV, og så øker Vt til 8mL/kg i ett minutt og noterer oss ny PPV. Vi noterer oss endringen, og så reduserer Vt tilbake til 6 mL/kg dersom pasienten har høy risiko for ventilatorindusert lungeskade (3). Ved å bruke tidal volume challange så flytter vi pasienten mot venstre på Frank-Starlingkurven ved ende-inspirasjon (punkt A på figuren over). Hvis vi er langt utpå det flate partier, vil ikke PPV endre seg. Hvis vi er på det bratte partiet, vil PPV øke. Det skal ikke store endringer til: en økning i PPV rundt 1 til 3,5 taler for at pasienten er væskeresponder.
Verdien av tidal volume challange har blitt bekreftet hos intensivpasienter med dårlig lungecompliance (4-7, 14), ARDS-pasienter i mageleie (8), pasienter til operasjon i ryggleie (9), operasjon i mageleie (10) og operasjon med laparoskopi i Trendelenburgs leie (11).
Problemet med tidal volume challenge er intuberte pasienter som er spontanpustende. Spontan pust gir uforutsigbare svingninger i preload, og reduserer presisjonen til PPV ved tidal volume challenge (12). Heldigvis er løsningen på dette rett rundt hjørnet.
PPV og passive leg raise (PLR)
Passiv beinheving (PLR) er foreløpig den eneste måten å undersøke om den spontanpustende pasienten er væskeresponder. Det innebærer at man måler pasientens slagvolum eller cardiac output i liggende stilling med overkroppen hevet 30-45 grader og beina flatt. Deretter tipper man sengen slik at pasienten ligger med overkroppen flatt og beina hevet 30-45 grader, for så å måle slagvolum eller cardiac output på nytt. PLR krever dermed en avansert hemodynamisk monitor til å beregne cardiac output, noe som få anestesileger har. I det siste året har det kommet to artikler (7,13) om å bruke PLR sammen med PPV, noe som lar oss bruke PLR med arteriekranen.
PLR hever preload, som flytter oss mot høyre på Frank-Starlingkurven. Dersom vi er på det bratte partiet, vil PPV falle, men dersom vi er på det flate pariet vil PPV ikke endre seg. Hvis PPV faller med 2 eller mer, taler dette for at pasienten er væskeresponder (7,13). I den siste studien gjaldt dette også for spontanpustende respiratorpasienter (13).
PPV etter 500 mL væskebolus
Dersom pasienten er på den bratte delen av Frank-Starlingkurven og du gir væske, skal PPV falle på samme måte som PLR. I studiene med PLR og PPV fikk pasientene som var væskerespondere 500mL væskebolus, og PPV falt med ca. 4, mens ikke-respondere falt rundt 1 (7,13). Dersom PPV ikke faller (og pasienten ikke blør fort) er pasienten ikke væskeresponder.
Vedvarende begrensninger med PPV
Jeg har ikke funnet noen på spontanpustende pasienter som ikke er på respirator. Fysiologien bak PPV er fremdeles gyldig, men svingningene i preload vil variere og dermed vil ikke cut-offene fra studiene gjelde. Likevel, dersom PPV øker under vakta taler det for at preload faller. Dersom PPV faller ved PLR, taler det for at pasienten er væskeresponder. Det vi ikke vet er cut-off verdiene på hvor mye endring i PPV som må til.
Atrieflimmer gir uregelmessig fylning av venstre ventrikkel og dermed uregelmessig pulstrykk. Maskinen oppgir ofte ikke PPV i det hele tatt.
PPV – Det store bilde
I realiteten er ikke pasientene enten væskeresponder eller ikke væskeresponder. Det er en gradert tilstand fra «veldig mye væskeresponder» til «veldig lite væskeresponder». Jo lengre unna man kommer de diagnostiske cut-off verdiene, jo mer eller mindre væskerespondere er de (14). Dette betyr at alle verdier av PPV kan brukes, så lenge man tolker de i riktig kontekst.
I enkelte tilfeller kan det være klokt å holde tilbake væske, til tross for at pasienten er væskeresponder. De gunstige effektene ved et væskebolus er kortvarige, og de negative effektene (i form av ødem) er langvarige. Tilstander som septisk sjokk og generalisert ødem gjør at de gunstige effektene varer enda kortere, og tilstander ved ødem eller høy CVP taler for at de negative effektene er enda større (14).
Det gir ingen mening med å gi væske til væskerespondere dersom vevsperfusjon er tilstrekkelig. Dessverre er dette et daglig fenomen: Mange bruker noradrenalindoser som et tegn på vevsperfusjon, hvor høye doser er farlig og skader pasienten. Dette er en misforståelse. Noradrenalin er indisert ved vasodilatasjon og forbedrer vevsperfusjonen i mange situasjoner. Å gi væske til en vasodilatert pasient fordi dosene med noradrenalin er dømt til å ende i volum overload. Det finnes mange tegn på vevsperfusjon, men det jeg liker best er dobbel blodgass som gir ScvO2, PvaCO2 og laktat (14). Andre tegn er MAP, cardiac output, hudstatus og kapillærfylning; mindre spesifikke er oliguri og mental status.
Det kan være viktigere å bruke væskerespons for diagnostikk av lav/høy preload enn å utløse væskeboluser.
Oppsummert kan PPV overvåke preload uten avanserte monitorer som ekko, PiCCO eller Swan-Ganz. På følgende måter forteller PPV at pasienten ikke er hypovolem og at væske er kontraindisert:
- PPV < 12 – hvis Vt er over 8mL/kg
- PPV faller med mindre enn 2 ved PLR
- PPV øker med mindre enn 2-3,5 ved tidal volum challenge
- PPV er det samme før og etter du har gitt væske.
- Vevsperfusjon er normal.
(Figur, samme som forsidebilde, hentet fra referanse 2)
Referanser
1. Yang X, Du B. Does pulse pressure variation predict fluid responsiveness in critically ill patients? A systematic review and meta-analysis. Critical Care. 2014 Nov 27;18(6):650.
2. Teboul JL, Monnet X, Chemla D, Michard F. Arterial Pulse Pressure Variation with Mechanical Ventilation. Am J Respir Crit Care Med. 2019 Jan 1;199(1):22–31.
3. Myatra SN, Monnet X, Teboul JL. Use of ‘tidal volume challenge’ to improve the reliability of pulse pressure variation. Critical Care. 2017 Mar 21;21(1):60.
4. Myatra SN, Prabu NR, Divatia JV, Monnet X, Kulkarni AP, Teboul JL. The Changes in Pulse Pressure Variation or Stroke Volume Variation After a “Tidal Volume Challenge” Reliably Predict Fluid Responsiveness During Low Tidal Volume Ventilation*. Critical Care Medicine. 2017 Mar;45(3):415–21.
5. Xu Y, Guo J, Wu Q, Chen J. Efficacy of using tidal volume challenge to improve the reliability of pulse pressure variation reduced in low tidal volume ventilated critically ill patients with decreased respiratory system compliance. BMC Anesthesiol. 2022 May 4;22(1):137.
6. Elsayed AI, Selim KA, Zaghla HE, Mowafy HE, Fakher MA. Comparison of Changes in PPV Using a Tidal Volume Challenge with a Passive Leg Raising Test to Predict Fluid Responsiveness in Patients Ventilated Using Low Tidal Volume. Indian J Crit Care Med. 2021 Jun;25(6):685–90.
7. Taccheri T, Gavelli F, Teboul JL, Shi R, Monnet X. Do changes in pulse pressure variation and inferior vena cava distensibility during passive leg raising and tidal volume challenge detect preload responsiveness in case of low tidal volume ventilation? Critical Care. 2021 Mar 18;25(1):110.
8. Shi R, Ayed S, Moretto F, Azzolina D, De Vita N, Gavelli F, et al. Tidal volume challenge to predict preload responsiveness in patients with acute respiratory distress syndrome under prone position. Crit Care. 2022 Jul 18;26(1):219.
9. Messina A, Montagnini C, Cammarota G, De Rosa S, Giuliani F, Muratore L, et al. Tidal volume challenge to predict fluid responsiveness in the operating room: An observational study. Eur J Anaesthesiol. 2019 Aug;36(8):583–91.
10. Messina A, Montagnini C, Cammarota G, Giuliani F, Muratore L, Baggiani M, et al. Assessment of Fluid Responsiveness in Prone Neurosurgical Patients Undergoing Protective Ventilation: Role of Dynamic Indices, Tidal Volume Challenge, and End-Expiratory Occlusion Test. Anesth Analg. 2020 Mar;130(3):752–61.
11. Jun JH, Chung RK, Baik HJ, Chung MH, Hyeon JS, Lee YG, et al. The tidal volume challenge improves the reliability of dynamic preload indices during robot-assisted laparoscopic surgery in the Trendelenburg position with lung-protective ventilation. BMC Anesthesiol. 2019 Aug 7;19(1):142.
12. Hamzaoui O, Shi R, Carelli S, Sztrymf B, Prat D, Jacobs F, et al. Changes in pulse pressure variation to assess preload responsiveness in mechanically ventilated patients with spontaneous breathing activity: an observational study. Br J Anaesth. 2021 Oct;127(4):532–8.
13. Mallat J, Fischer MO, Granier M, Vinsonneau C, Jonard M, Mahjoub Y, et al. Passive leg raising-induced changes in pulse pressure variation to assess fluid responsiveness in mechanically ventilated patients: a multicentre prospective observational study. British Journal of Anaesthesia [Internet]. 2022 Jul 14 [cited 2022 Jul 26];0(0). Available from: https://www.bjanaesthesia.org/article/S0007-0912(22)00309-9/fulltext
14. Monnet X, Shi R, Teboul JL. Prediction of fluid responsiveness. What’s new? Annals of Intensive Care. 2022 May 28;12(1):46.